在過(guò)去的十年中,癌癥免疫治療領(lǐng)域取得了顯著進(jìn)展�。免疫系統(tǒng)檢查點(diǎn)抑制劑的發(fā)現(xiàn)和雙特異性抗體�����、特異性阻斷抗體、過(guò)繼細(xì)胞療法或細(xì)胞因子的后續(xù)使用使我們能夠從不同的角度面對(duì)癌癥�,其中療法使用免疫細(xì)胞識(shí)別和殺死腫瘤細(xì)胞的能力���。
盡管取得了這些進(jìn)展,但仍有許多類型的腫瘤對(duì)免疫療法沒(méi)有反應(yīng)�。腫瘤基質(zhì)的復(fù)雜性、其異常脈管系統(tǒng)�����、代謝限制�、免疫抑制細(xì)胞向腫瘤床的募集以及免疫抑制微環(huán)境的產(chǎn)生是免疫系統(tǒng)對(duì)其抗腫瘤作用必須面對(duì)的巨大障礙?�;谧詳U(kuò)增RNA(saRNA)的病毒載體可以產(chǎn)生高和瞬時(shí)水平的轉(zhuǎn)基因表達(dá)并誘導(dǎo)先天免疫應(yīng)答����,使其成為抗腫瘤治療的有趣工具。這些載體通常以病毒顆粒的形式遞送����,但也可以以RNA的形式施用。
近日�,納瓦拉CIMA大學(xué)的研究人員在《分子療法》雜志上發(fā)表了一篇題為《Intratoral
electroporation of a self-amplified RNA expressing IL-12 induces
antuminocular effects in mouse models of
cancer》的文章���。研究表明��,通過(guò)電穿孔局部遞送saRNA可能是癌癥免疫治療的有吸引力的策略�����。這種方法可以很容易地轉(zhuǎn)化為臨床實(shí)踐��,特別是對(duì)于皮膚可以觸及的腫瘤���。
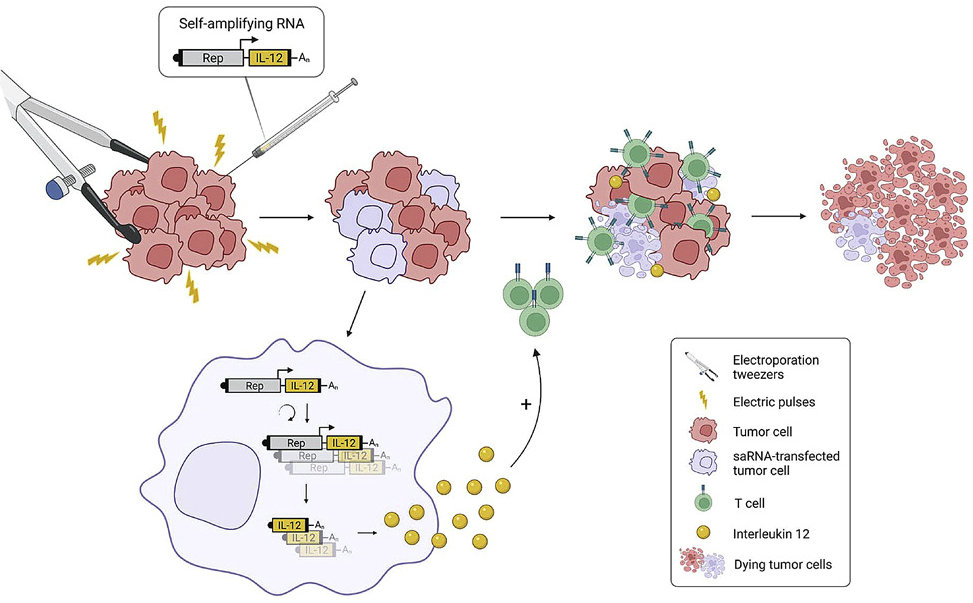
在這項(xiàng)研究中��,研究人員通過(guò)體內(nèi)電穿孔Semliki Forest病毒(SFV)saRNA以局部治療小鼠結(jié)直腸MC38皮下腫瘤來(lái)評(píng)估這種可能性����。編碼熒光素酶的SFV載體用于優(yōu)化腫瘤中saRNA電穿孔的條件����。
然后,研究人員使用SFV
saRNA評(píng)估了這種方法的治療潛力���,SFV
saRNA編碼白細(xì)胞介素-12(SFV-IL-12)����,這是一種具有強(qiáng)烈抗腫瘤作用的促炎細(xì)胞因子。通過(guò)使用我們用SFV-IL-12
RNA的最佳電穿孔條件�,研究人員能夠在MC 38結(jié)腸腺癌和PM299 L
HCC腫瘤中誘導(dǎo)顯著的抗腫瘤作用。在電穿孔之前通過(guò)向腫瘤注射透明質(zhì)酸酶來(lái)高度增強(qiáng)這種作用����。這種酶可以降解腫瘤中存在的富含HA的基質(zhì),可能允許saRNA的更好分布�����,電穿孔后���,saRNA可以接近更多數(shù)量的細(xì)胞�����。
事實(shí)上�����,研究人員之前已經(jīng)觀察到MC 38腫瘤可以表達(dá)PD-L1���,這可能會(huì)抑制抗腫瘤反應(yīng)。因此���,SFV-IL-12電穿孔與抗PD-I單克隆抗體(mAb)的組合能夠進(jìn)一步增強(qiáng)該療法的治療效果�。
先前的研究已經(jīng)證明��,腫瘤內(nèi)遞送表達(dá)抗PD-Ll的SFVVP(SFV-aPD-Ll)可誘導(dǎo)有效的抗腫瘤作用�。因此,在未來(lái)的實(shí)驗(yàn)中測(cè)試電穿孔的SFV-aPD-Ll
RNA是否也可以產(chǎn)生治療效果將是有趣的����。總之�,本研究的結(jié)果表明,通過(guò)電穿孔遞送sRNA可能是局部癌癥免疫治療的一個(gè)有吸引力的策略���。這種方法可以更容易地轉(zhuǎn)化為臨床實(shí)踐�����,特別是對(duì)于經(jīng)皮可達(dá)的腫瘤���。
分子細(xì)胞生物學(xué)實(shí)驗(yàn)











 實(shí)驗(yàn)熱線:4006991663
實(shí)驗(yàn)熱線:4006991663